选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
试题详情
化学与生活密切相关,下列说法错误的是( )
- A、 节日燃放的烟花与电子的跃迁有关
- B、 用纯碱作洗涤剂利用了盐类水解原理
- C、 电解质水饮料中含有水、氯化钠、葡萄糖等多种电解质
- D、 两种不同金属材质的电线相接易发生腐蚀
试题详情
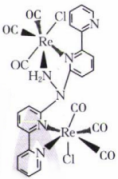
2023年4月12日21时,中国有“人造太阳”之称的全超导托卡马克核聚变实验装置(EAST)创造了新的世界纪录,成功实现稳态高约束模式等离子体运行403秒,对提升核聚变能源经济性、可行性,加快实现聚变发电具有重要意义。其原理为 , 下列有关说法正确的是( )
, 下列有关说法正确的是( )
- A、 聚变发电有利于减少碳排放量
- B、 核聚变为放热反应
- C、 聚变发电,可使核能全部转化成电能
- D、
、
互为同素异形体
试题详情
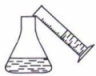
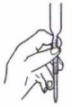
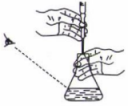
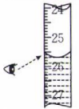
下列有关以0.1 mol·L NaOH标准液滴定未知浓度的HCl溶液的操作正确的是( )
NaOH标准液滴定未知浓度的HCl溶液的操作正确的是( )
|
|
|
|
A.量取25.00 mL待测液 | B.除去碱式滴定管中的气泡 | C.滴定时,眼睛注视锥形瓶内溶液颜色的变化 | D.滴定结束时读数 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
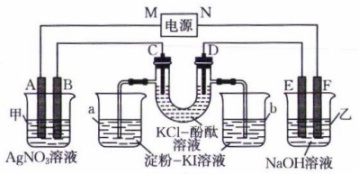
如图所示,A、B、C、D、E、F均为石墨电极,甲池与乙池中溶液的体积均为0.2 L,浓度均为1 mol⋅L , 按图示接通电路,反应一段时间后,检测到电路中通过0.02 mol
, 按图示接通电路,反应一段时间后,检测到电路中通过0.02 mol  , 烧杯a中溶液变蓝。下列说法正确的是( )
, 烧杯a中溶液变蓝。下列说法正确的是( )
- A、 M为电源负极
- B、 C极与E极产生的气体质量差为0.55 g
- C、 烧杯b中溶液颜色变为浅红色
- D、 忽略体积变化,甲池中溶液的
试题详情
超分子因其特殊结构在某些方面有着重要应用。超分子化学已成为今后化学发展的另一个全新的领域。月桂酰丙氨酸形成超分子结构的过程如图。下列说法错误的是( )
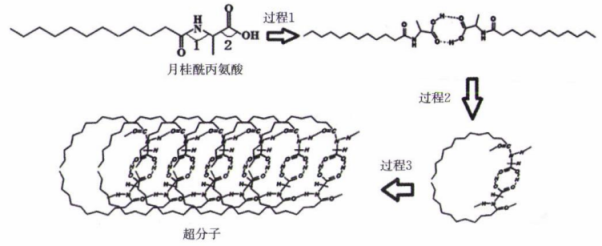
- A、 该超分子中含有的化学键有极性键、非极性键、氢键
- B、 月桂酰丙氨酸中键角:
- C、 以上三个过程表现了超分子的自组装特征
- D、 超分子中形成的空腔能识别某些分子或离子
试题详情
肼( )是一种强还原剂,在碱性溶液中能将银、镍等金属离子还原成金属单质,因此可用于镜面镀银,原理为
)是一种强还原剂,在碱性溶液中能将银、镍等金属离子还原成金属单质,因此可用于镜面镀银,原理为 。下列说法正确的是( )
。下列说法正确的是( )
- A、 Ag为d区元素
- B、 肼分子中心原子的VSEPR模型为四面体形
- C、 肼分子结构对称,为非极性分子
- D、 肼与氨气的组成元素相同,性质也完全相同
试题详情
某化合物的晶胞结构示意图如图,晶胞参数为a nm,设 为阿伏加德罗常数的值,以晶胞参数建立坐标系,1号原子的坐标为
为阿伏加德罗常数的值,以晶胞参数建立坐标系,1号原子的坐标为 , 3号原子的坐标为
, 3号原子的坐标为 。下列说法错误的是( )
。下列说法错误的是( )
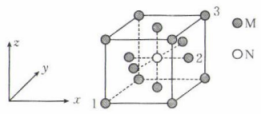
- A、 晶体中M、N的个数比为4∶1
- B、 2号原子的坐标为
- C、 M、N之间的最短距离为
nm
- D、 位于面心的M围成正八面体
试题详情
常温下,向100 mL 0.1 mol·L 三元酸
三元酸 溶液中滴加0.1 mol⋅L
溶液中滴加0.1 mol⋅L 的NaOH溶液,溶液中含A微粒的物质的量分数(δ)随溶液pH的变化如图所示,下列说法正确的是( )
的NaOH溶液,溶液中含A微粒的物质的量分数(δ)随溶液pH的变化如图所示,下列说法正确的是( )
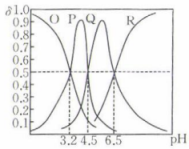
- A、 P为HA的物质的量分数与溶液pH的关系曲线
- B、 该三元酸的第一步电离是完全的
- C、 当加入100 mL NaOH溶液时,溶液显酸性
- D、 常温下,
的水解常数
非选择题:本题共4小题,共55分。
试题详情
某农药由原子序数依次增大的V、W、X、Y、Z五种前四周期元素组成。请根据下列相关信息,回答问题。
元素 | 相关信息 |
V | 核外电子数与周期序数相等 |
W | 成对电子数与未成对电子数之比为3∶1 |
X | 在火山口附近可发现其淡黄色固体单质 |
Y | 有四个电子层,且最外层电子数与最内层电子数相等 |
Z | 基态Z元素原子的价层电子排布式为 |
试题详情
某化学兴趣小组用如图装置探究反应 的进行程度。
的进行程度。
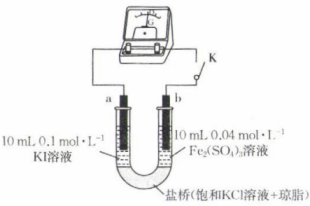
已知:①a、b均为石墨电极;②实验中使用的电流计有电流通过时,指针偏向正极;③空气不影响该实验。
试题详情
硫酸锌是制造锌钡白和锌盐的主要原料,口服硫酸锌可纠正锌缺乏,恢复酶系统的功能。用锌白矿(主要成分为ZnO,还含有 、
、 、
、 等杂质)制备
等杂质)制备 的流程如图:
的流程如图:
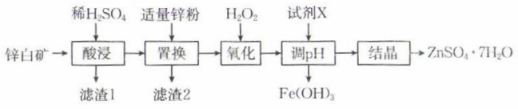
常温下,相关金属离子形成氢氧化物沉淀的pH如表所示(离子浓度小于mol⋅L
时视为沉淀完全):
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
1.1 | 3.1 | |
7.6 | 9.6 | |
6.4 | 8.0 |
试题详情
C、Si、Ge、Sn是同族元素,该族元素的单质及其化合物在材料、医药等方面有重要应用。请回答下列问题: