单选题
试题详情
如图所示,有关化学反应和能量变化的说法正确的是( )
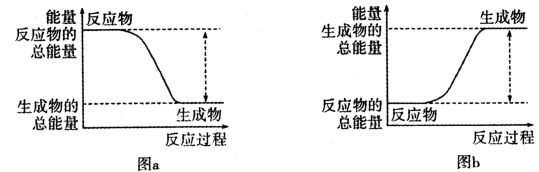
- A、 图a表示的是吸热反应的能量变化
- B、 图b中反应物比生成物稳定
- C、 图a可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
- D、 图a中的反应不需要加热就一定能发生,图b中的反应一定需要加热才能发生
试题详情
利用固体表面催化工艺进行NO分解的过程如下图所示。
![]()
下列说法错误的是( )
- A、 NO属于共价化合物
- B、 O2含有非极性共价键
- C、 过程②吸收能量,过程③释放能量
- D、 标准状况下,NO分解生成11.2LN2转移电子数为6.02×1023
试题详情
锂海水电池的反应原理为:2Li+2H2O=2LiOH+H2↑,其示意图如图所示。有关该电池工作时说法错误的是( )

- A、 金属锂作正极
- B、 镍电极上发生还原反应
- C、 海水作为电解质溶液
- D、 可将化学能转化为电能
试题详情
反应C(s)+H2O(g)  CO(g)+H2(g)在一体积可变 的密闭容器中进行。改变下列条件对提高化学反应速率比较明显的是( )
CO(g)+H2(g)在一体积可变 的密闭容器中进行。改变下列条件对提高化学反应速率比较明显的是( )
①增大C的用量;②将容器体积缩小一半;③保持压强不变,充入N2使容器体积增大;④温度升高;⑤保持体积不变,充入水蒸气
- A、 ②④
- B、 ①③
- C、 ②④⑤
- D、 ①④
试题详情
已知短周期元素的离子aA2+、bB+、cC3-、dD-具有相同的电子层结构。则下列叙述正确的是( )
- A、 原子半径:A>B>D>C
- B、 原子序数:d>c>b>a
- C、 原子的最外层电子数:C>D>A>B
- D、 离子半径:C3->D->B+>A2+
试题详情
下列反应的离子方程式书写正确的是( )
- A、 用氯化铁溶液腐蚀铜电路板:Cu +2Fe3+=Cu2++ 2Fe2+
- B、 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
- C、 向稀硫酸中加入Ba(OH)2溶液:Ba2++OH-+ H++ SO
=BaSO4↓+ H2O
- D、 向AlCl3溶液中加入过量氨水:Al3++ 4NH3·H2O=4NH
+AlO
+2H2O
试题详情
某有机物的结构简式如下图所示。下列有关该有机物的叙述正确的是( )

- A、 该有机物的分子式为C11H14O2
- B、 1 mol该有机物在Ni作催化制的条件下能与4 mol H2发生加成反应
- C、 该有机物最多消耗NaOH与Na的物质的量之比为2:1
- D、 该有机物共有三种官能团,分别为:碳碳双键、羟基、羰基
试题详情
为了从海带浸取液中提取碘,某同学设计了如下实验方案:
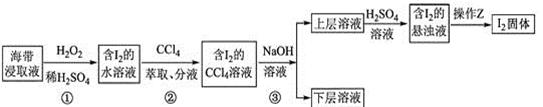
下列说法正确的是( )
- A、 ①中反应的离子方程式:2I− + H2O2=I2 + 2OH−
- B、 ②中分液时含I2的CCl4溶液从分液漏斗上口倒出
- C、 ③中得到的上层溶液中含有I−
- D、 操作Z的名称是加热
试题详情
下列实验操作、现象、得出的结论均正确的是( )
| 实验 | 结论 | |
| A | 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 | 生成的一氯甲烷具有酸性 |
| B | 向淀粉水解的产物中直接加入新制的氢氧化铜悬浊液,并加热煮沸,没有出现砖红色沉淀 | 水解的产物无还原性 |
| C | 室温下,向浓度为0.2 mol/L的BaCl2溶液中通入CO2气体,出现白色沉淀 | CO2与BaCl2反应生成BaCO3沉淀 |
| D | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的1,2-二溴乙烷无色、可溶于四氯化碳 |
- A、 A
- B、 B
- C、 C
- D、 D
实验题
推断题
试题详情
下列是元素周期表一部分,其中①~⑩序号各代表一种元素,请回答下列问题:

填空题
试题详情
发射卫星时可用肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。
解答题
试题详情
在2L绝热密闭容器中投入2molSO2和bmolO2 , 下图是部分反应物随时间的变化曲线。

①10 min时,v(SO3)=。
②反应达到平衡时,SO2的转化率为。
③下列情况能说明该反应达到化学平衡的是。
A.v(SO3)=v(SO2) B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变 D.混合气体的总物质的量不再改变
综合题
试题详情
氯及其化合物在生产生活中都有重要的应用。
工业流程
试题详情
明矾在日常生活中用途非常广泛。用废铝灰(含Al、Al2O3、Fe、Fe2O3、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:

已知:Fe3+开始沉淀到沉淀完全时溶液的pH为1.9~3.7。



