选择题(本题共20小题,1-10题每题2分,11-20题每题3分。在下列各题的四个选项中,只有一项是最符合题意的。)
试题详情
化学与生活密切相关,下列说法正确的是( )
- A、 氢氧化铝胶体可用来对自来水净化和杀菌消毒
- B、 “血液透析”利用了胶体丁达尔效应
- C、 BaSO4常用来作胃镜中的“钡餐”
- D、 为了消除碘缺乏病,在食用盐中加入一定量的碘单质
试题详情
两种溶液相互滴加,反应过程中现象完全相同但离子方程式不同的是( )
- A、 NaHCO3溶液与Ca(OH)2溶液
- B、 Na2CO3溶液与稀盐酸
- C、 Ca(HCO3)2溶液与Ca(OH)2溶液
- D、 AlCl3溶液与NaOH溶液
试题详情
欲配制100mL1.0mol·L-1硫酸钠溶液,不正确的方法是( )
- A、 将14.2g硫酸钠溶于100mL水中
- B、 将32.2gNa2SO4·10H2O溶于少量水中,再加水稀释至100mL
- C、 将20mL5.0mol·L-1硫酸钠溶液用水稀释至100mL
- D、 将14.2g硫酸钠溶于水中得到100mL溶液
试题详情
已知拆开1molH-H键,1molN=N键分别需要吸收的能量为436kJ、946kJ;形成1molN-H键,会放出能量391kJ,在反应 中,每生成3molN-H键( )
中,每生成3molN-H键( )
- A、 吸收92kJ热量
- B、 放出46kJ热量
- C、 放出209kJ热量
- D、 吸收209kJ热量
试题详情
设NA为阿伏加德罗常数的值,下列说法正确的是( )
- A、 一定量的钠与8g氧气反应,若两者均无剩余,转移电子的数目为NA
- B、 等物质的量的14NO和13CO气体中所含中子数均为15NA
- C、 1mol丙烯酸(CH2=CHCOOH)中含有双键的数目为NA
- D、 常温下,100mLpH=1的醋酸溶液中含有的氢离子数目为0.01NA
试题详情
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193R,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是( )
- A、 S2Cl2是含有极性键和非极性键的非极性分子
- B、 固态时S2Cl2属于共价晶体
- C、 S2Cl2与NaOH的化学方程式可能为:
- D、 S2Cl2的电子式为
试题详情
CO2与SO2都是酸性氧化物,有许多相似的化学性质。用X表示C或S元素,下列反应的离子方程式一定正确的是( )
- A、 使用过量的氨水吸收:
- B、 将少量的XO2通入漂白粉溶液中:
- C、 XO2溶于水:
- D、 将过量的XO2通入NaOH溶液中:
试题详情
甲~庚等元素在周期表中的相对位置如下表。己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
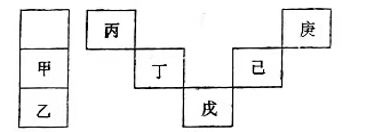
- A、 丙与戊的原子序数相差28
- B、 气态氢化物的稳定性:庚<己<戊
- C、 常温下,甲和乙的单质均能与水剧烈反应
- D、 丁的最高价氧化物可用于制造半导体材料
试题详情
某无色澄清溶液可能含有Na+、Mg2+、Al3+、Ba2+、Fe3+、Cl-、SO42-、CO32-中的若干种,取样分别进行如下实验:
①逐滴加入NaOH溶液,有白色沉淀生成,继续滴加至过量,沉淀部分溶解。
②加足量BaCl2溶液,产生白色沉淀,再向沉淀中加入过量稀盐酸,沉淀质量不变。
下列说法错误的是( )
- A、 原溶液中一定存在SO42-、Mg2+、Al3+
- B、 原溶液中可能存在Na+、Ba2+、Cl-
- C、 原溶液中一定不存在Ba2+、Fe3+、CO32-
- D、 原溶液中可能存在Na+、Cl-
试题详情
某工厂拟综合处理含NH4+的废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计如图所示流程:
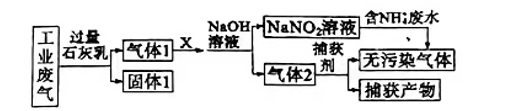
下列说法不正确的是( )
- A、 固体I中主要含有CaCO3、CaSO3、Ca(OH)2
- B、 X可以是空气,但不能过量
- C、 捕获剂所捕获的气体主要是CO、N2
- D、 处理含NH4+废水时,发生的反应为
试题详情
为确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入30.0mL某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是( )
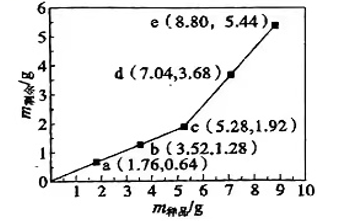
- A、 各组样品均发生反应:
、
- B、 1.76g样品充分反应后,溶液中一定存在Fe2+和Cu2+ , 一定不存在Fe3+
- C、 该混合物中n(Fe2O3):n(Cu)=3:1
- D、 稀硫酸的浓度为1.5mol·L-1
试题详情
金合欢醇广泛应用于多种香型的香精中,其结构简式如图所示。下列说法不正确的是( )
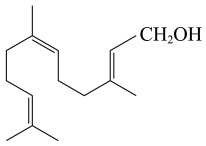
- A、 金合欢醇的同分异构体中不可能有芳香烃类
- B、 金合欢醇可发生加成反应、取代反应、氧化反应
- C、 金合欢醇分子的分子式为C15H26O
- D、 1 mol金合欢醇与足量Na反应生成0.5 mol氢气, 与足量NaHCO3溶液反应生成1 mol CO2
试题详情
碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
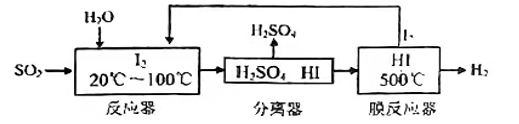
下列说法正确的是( )
- A、 分离器中的物质分离操作为过滤
- B、 膜反应器中,加入催化剂可以改变该反应的焓变
- C、 该工艺中I2和HI的相互转化体现了“碘循环”
- D、 碘循环工艺的总反应为
试题详情
将0.1molCl2通入100mL含等物质的量的HBr与H2SO3的混合溶液中,有一半的HBr被氧化,则下列说法正确的是( )
- A、 物质的还原性:HBr>H2SO3>HCl
- B、 HBr与H2SO3的物质的量浓度均为0.6mol·L-1
- C、 通入0.1molCl2发生反应的离子方程式为
- D、 若再通入0.05molCl2 , 恰好能将HBr和H2SO3完全氧化
试题详情
已知:溴化铁在200℃以上易分解,煮沸水溶液也会使其分解,生成溴化亚铁和溴单质。实验室里利用如图装置制取纯净的无水FeBr3。
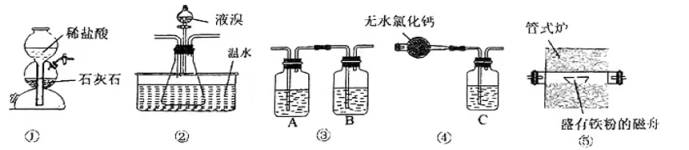
下列说法正确的是( )
- A、 A、B、C分别盛有饱和Na2CO3溶液、浓硫酸和烧碱溶液
- B、 实验结束时,先停止加热并停止滴入液溴,继续通入CO2至室温
- C、 实验开始时,先加热管式炉,再打开装置①中活塞
- D、 装置②中温水的作用是降低装置①中生成的CO2在液溴中的溶解度
试题详情
某化工厂制备净水剂硫酸铁铵晶体【NH4Fe(SO4)2·6H2O】的一种方案如下:

下列说法不正确的是( )
- A、 滤渣A的主要成分是CaSO4
- B、 “合成”反应要控制温度,温度过高,产率会降低
- C、 “系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等
- D、 相同条件下,NH4Fe(SO4)2·6H2O净水能力比FeCl3强
试题详情
某种固体消毒剂广泛用于游泳池消毒,其结构如图所示,其中W、X、Y、7是原子序数依次增大的四种短周期元素,Y的最外层电子数是内层电子数的3倍。下列叙述错误的是( )
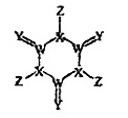
- A、 W和Z组成的化合物可以作灭火剂
- B、 原子半径:W>X>Y
- C、 氧化物对应的水化物的酸性:Z>X
- D、 该化合物中X、Y、Z均满足8电子稳定结构
非选择题
试题详情
四氯化锡(SnCl4)是一种重要的化工原料,主要用于有机锡化合物的制造,也可用作分析试剂、有机合成脱水剂等。已知锡单质在加热时可直接与氯气化合生成,某实验小组用如下装置对其进行合成。
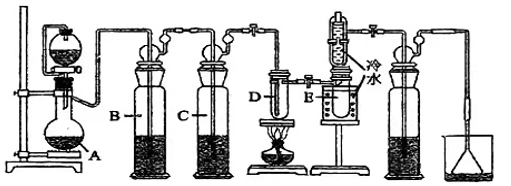
【相关药品性质】
药品 | 颜色、状态 | 熔点(℃) | 沸点(℃) | 其他性质 |
Sn | 银白色固体 | 231 | 2260 | 较活泼金属能与O2、HCl等气体发生反应 |
SnCl4 | 无色液体 | -33 | 114 | 极易水解产生SnO2.xH2O溶胶 |
请回答下列问题:
试题详情
氧化铈(CeO2)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示:
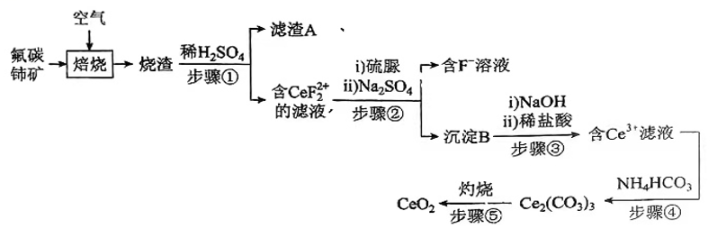
已知:①稀土离子易与SO42-形成复盐沉淀,Ce3+和SO42-发生反应:;
②硫脲:具有还原性,酸性条件下易被氧化为(SCN2H3)2;
③Ce3+在空气中易被氧化为Ce4+ , 两者均能形成氢氧化物沉淀;
④Ce2(CO3)3为白色粉末,难溶于水。
回答下列问题:
试题详情
已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个国家的石油化工发展水平。下列是有机物A~G之间的转化关系:
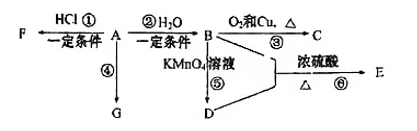
请回答下列问题:


