选择题
试题详情
下列叙述I和II均正确并且有因果关系的是( )
选项 | 叙述I | 叙述II |
A | | 用 |
B | | 可加热 |
C | | 可用 |
D | | |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
将43.8g Al、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44LNO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为( )
- A、 39.2g
- B、 44.8g
- C、 58.8g
- D、 66.4g
试题详情
取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为 ),反应现象没有明显差别的是
),反应现象没有明显差别的是
| 选项 | 试剂① | 试剂② |
| A | 氨水 |
|
| B |
|
|
| C |
| 酸性 |
| D |
|
|
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
某同学用KSCN溶液和FeCl2溶液探究Fe2+的还原性时出现异常现象,实验如下:
| ① | ② | ③ |
| | | |
| 溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀 | 溶液变红且不褪色,有气体生成(经检验为O2),经检验有丁达尔效应。 | 溶液变红且不褪色,滴加盐酸和BaCl2溶液,无白色沉淀,经检验无丁达尔效应。 |
下列说法错误的是( )
- A、 ②中红色溶液中含有Fe(OH)3胶体
- B、 实验②中发生的氧化还原反应只有两种
- C、 对比①②③,可以判定酸性条件下H2O2可以氧化SCN-
- D、 ③中发生的氧化还原反应为:4Fe2++O2+4H+=4Fe3++2H2O
试题详情
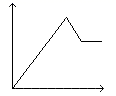
向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液。下列图象中能符合题意表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)( )
- A、
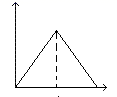
- B、

- C、
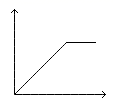
- D、
试题详情
已知还原性 。向一定体积的
。向一定体积的 和
和 混合溶液中通入氯气,测得溶液中离子的物质的量随氯气体积的变化曲线如图所示(e和g点横坐标分别为2.5和4.5)。下列说法正确的是 ( )
混合溶液中通入氯气,测得溶液中离子的物质的量随氯气体积的变化曲线如图所示(e和g点横坐标分别为2.5和4.5)。下列说法正确的是 ( )
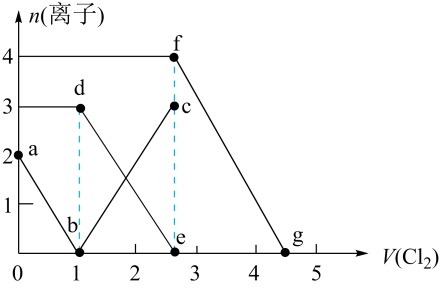
- A、 ab段表示
物质的量的变化情况
- B、 原溶液中
和
的物质的量分别为
、
- C、 fg段发生反应:
- D、 反应
能发生
多选题
试题详情
某同学将 钾投入
钾投入 溶液中,待其充分反应。下列叙述错误的是( )
溶液中,待其充分反应。下列叙述错误的是( )
试题详情
在托盘天平的两盘,放上质量相等的A、B两烧杯,调至平衡,然后分别倒入质量相等的足量盐酸,继而在AB两烧杯中放入下述各组物质,结果天平仍保持平衡的是( )
试题详情
利用废旧镀锌铁皮制备 胶体粒子的流程如图。
胶体粒子的流程如图。
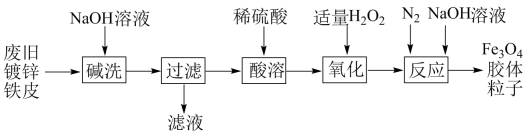
已知:Zn溶于强碱时生成可溶于水的
下列有关说法不正确的是( )
非选择题
试题详情
钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
试题详情
某工厂的酸性废水中主要含有 、
、 等离子,为了减少污染并变废为宝,工程师设计了如下流程,回收铜和绿矾(FeSO4·7H2O)。
等离子,为了减少污染并变废为宝,工程师设计了如下流程,回收铜和绿矾(FeSO4·7H2O)。

试题详情
某同学按下表操作,当物质充分反应后,最终发现仅有一个烧杯中有固体剩余。
| 烧杯编号 | ① | ② | ③ |
| 盛装的液体 |
|
|
|
| 加入的固体(质量相等) |
|
|
|
试题详情
物质可根据其组成和性质进行分类:
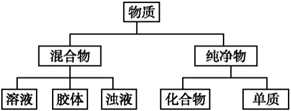
试题详情
某校研究性学习小组用一些大部分已经锈蚀(成分为 Fe2O3)的废铁屑制备绿矾(FeSO4·7H2O),实验操作过程如下:

已知:杂质不溶于稀硫酸。
请回答下列问题:
试题详情
过去电子工业常用30%的FeCl3溶液腐蚀覆有铜箔的绝缘板,制成印刷线路板,发生反应的化学方程式为3FeCl3+Cu=2FeCl2+CuCl2。
试题详情
铁是人类迄今为止人类冶炼和使用最多的金属。铁在人们的生产生活,乃至于国防、现代化建设中均发挥着极其重要的作用。
试题详情
某实验小组同学用KSCN探究久置  固体变质的情况。将0.3 g
固体变质的情况。将0.3 g  固体用10mL蒸馏水溶解,配成待测液,进行实验。
固体用10mL蒸馏水溶解,配成待测液,进行实验。






