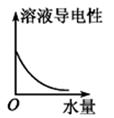
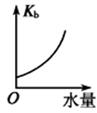
选择题:本题共16小题,共44分。(第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
试题详情
我国提出争取在2030年前实现碳达峰,2060年 实现碳中和,这对于实现绿色发展至关重要。为了实现“碳达峰”和“碳中和”,太阳能的利用逐渐得到重视。下列说法错误的是( )
- A、 煤、石油和天然气都属于碳素燃料
- B、 发展太阳能经济有助于减缓温室效应
- C、 太阳能电池可将太阳能直接转化为电能
- D、 太阳能的直接利用只有“光—电转换”和“光—生物质能转换”两种形式
试题详情
某反应的反应机理、能量与反应进程的关系如下图所示,下列说法正确的是( )

- A、
是该反应的催化剂
- B、 该反应焓变△H<0可知,该反应可自发进行
- C、 加入催化剂后,反应的△H变小
- D、 第一步反应的活化能比第二步反应的小
试题详情
反应C(s)+H2O(g) CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
- A、 升高温度
- B、 增加C(s)的量
- C、 将容器的容积缩小一半
- D、 压强不变,充入He使容器容积增大
试题详情
下列事实不能用勒夏特列原理解释的是( )
- A、 打开可乐瓶盖后看到有大量气泡逸出
- B、 H2、I2、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深
- C、 新制的氯水在光照条件下颜色变浅,溶液的pH减小
- D、 合成氨工业使用高压以提高氨的产量
试题详情
已知: 时,
时, ;
; 时,
时, 。下列有关水的电离的叙述正确的是( )
。下列有关水的电离的叙述正确的是( )
- A、 c(H+)随着温度的升高而减小
- B、
时,c(H+)>c(OH-)
- C、 向蒸馏水中加入
溶液,
增大
- D、 加入少量固体CuSO4,水的电离平衡正向移动
试题详情
下表中实验操作、现象与结论对应关系正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 以酚酞为指示剂,用盐酸标准液滴定氢氧化钠溶液 | 溶液由红色变为浅红色便立刻读数 | 测得c(NaOH)偏大 |
B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 有白色沉淀生成,溶液红色变浅 | 纯碱溶液呈碱性是由 |
C | 测定等浓度的NaClO溶液、CH3COONa溶液的pH | 前者大 | 酸性:HClO>CH3COOH |
D | 除去锅炉中沉积的CaSO4用饱和Na2CO3溶液浸泡,再用稀盐酸溶解除去 | 白色沉淀溶解 | CaSO4比CaCO3的 |
- A、 A
- B、 B
- C、 C
- D、 D
试题详情
NA表示阿伏加德罗常数的值,下列说法正确的是( )
- A、 常温下,pH=1的硫酸溶液中,含有H+数目为0.1NA
- B、 常温下,1 L 0.5 mol·L-1的AlCl3溶液中,含有Al3+数目为0.5NA
- C、 常温下,1 L pH=12的CH3COONa溶液,由水电离产生的OH-数目为0.01NA
- D、 标准状况下,4.48 L NH3溶于水得到的溶液中,NH3·H2O的总数为0.2NA
试题详情
25˚C时,下列有关电解质溶液的说法正确的是( )
- A、 0.1mol/L NaHCO3溶液中:c(Na+)=c(
)+c(
)
- B、 将CH3COONa溶液从25˚C升温至60˚C,溶液中
增大
- C、 直接加热FeCl3溶液可得到FeCl3固体
- D、 物质的量浓度相同的①NH4Cl溶液 ②NH4HCO3溶液,c(
):①>②
试题详情
根据下列图示所得出的结论正确的是:( )

- A、 图1表示反应2CO(g)+2NO(g)
N2(g)+2CO2(g)在其他条件不变时,起始CO物质的量与平衡时N2的体积分数关系,说明NO的转化率b>c>a
- B、 图2表示反应2X(g)
Y(g)分别在T1、T2温度下,Y的体积分数随时间的变化,说明该反应的ΔH<0
- C、 图3是室温下BaSO4达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO42-)的关系曲线,说明通过蒸发浓缩可使溶液由n点转化到m点
- D、 图4表示含少量SO2的水溶液暴露在空气中,溶液的pH随时间的变化,说明在空气中时间越长,亚硫酸的电离程度越大
试题详情
常温时,向 的
的 溶液中逐滴滴加
溶液中逐滴滴加 的
的 溶液,滴入
溶液,滴入 溶液的体积与溶液
溶液的体积与溶液 的变化如图所示。下列说法正确的是( )
的变化如图所示。下列说法正确的是( )
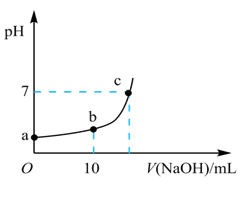
- A、 该滴定过程应该选择甲基橙作为指示剂
- B、 b点时,
- C、 c点时,
- D、 反应过程中,
的值不断增大
试题详情
执法交警最常用的一种酒精检测仪的工作原理示意图如图所示,其反应原理为CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法不正确的是( )

- A、 电解质溶液中的
移向a电极
- B、 b为正极,电极反应式为O2+2H2O+4e-=4OH-
- C、 呼出气体中酒精含量越高,微处理器中通过的电流越大
- D、 外电路中电子的移动方向为a→b
试题详情
硫化汞(HgS)是一种难溶于水的红褐色颜料,其在水中的沉淀溶解平衡曲线如图所示(已知T1<T2),下列说法错误的是( )

- A、 图中a点对应的是T2温度下HgS的不饱和溶液
- B、 图中各点对应的Ksp的关系为:p<q
- C、 向p点的溶液中加入少量Hg(NO3)2固体,p点向a点的转化
- D、 升高温度,可实现p点向q点的转化
试题详情
一定条件下,6H2(g) + 2CO2(g) C2H5OH(g) + 3H2O(g),
C2H5OH(g) + 3H2O(g), 平衡转化率随温度变化如图所示,对a、b、c 三点对应情况的分析,合理的是( )
平衡转化率随温度变化如图所示,对a、b、c 三点对应情况的分析,合理的是( )

- A、
物质的量分数:
- B、
物质的量:
- C、 平衡常数:
- D、 反应速率:
非选择题(共56分)
试题详情
甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g)CH3OH(g) ΔH1<0 K1
②2CH3OH(g)CH3OCH3(g)+H2O(g) ΔH2<0 K2
③CO(g)+H2O(g)CO2(g)+H2(g) ΔH3<0 K3
试题详情
以石膏矿(主要含2CaSO4•H2O,还含有少量Al2O3、Fe2O3、SiO2)为原料制取CaCl2溶液和(NH4)2SO4晶体,一种工艺流程如下:
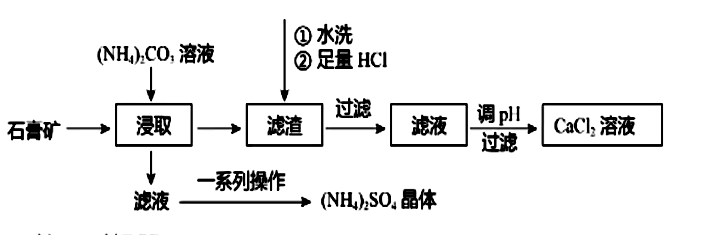
试题详情
根据要求回答问题:
试题详情
维生素C(C6H8O6 , M=176)具有重要生理调节功能,在酸性介质中较为稳定,在碱性溶液中易被空气氧化。维生素C通常用I2标准溶液进行滴定,反应原理是:
C6H8O6+I2═C6H6O6+2H++2I﹣ . 回答下列问题: